腫瘤免疫治療
1. 腫瘤免疫治療
腫瘤免疫治療(Cancer Immunotherapy)為現代癌症治療的一大突破。癌細胞之所以難纏,乃因癌細胞非常擅長偽裝,能產生一些蛋白質來欺騙免疫細胞,讓免疫系統誤以為它們是正常的身體組織,進而避開攻擊。腫瘤免疫治療與傳統的化療或放療直接攻擊癌細胞不同,免疫治療的核心邏輯為重新啟動或加強患者自身的免疫系統,讓身體的免疫大軍足以識別並消滅癌細胞。現行常見的治療方式有三種,分別為免疫檢查點抑制劑、CAR-T 療法、腫瘤微環境調控劑。
三種治療方式的核心概念在於針對不同免疫表型之腫瘤(immune phenotypes)進行精準調控,使「免疫活化型腫瘤(熱腫瘤)」與「免疫缺失型腫瘤(冷腫瘤)」皆能獲得有效治療。所謂熱腫瘤,是指腫瘤內其實已有許多T細胞存在,但這些免疫細胞受到抑制訊號(如免疫檢查點分子或抑制性細胞族群)影響,無法正常發揮其攻擊癌細胞的功能;而冷腫瘤則缺乏T細胞浸潤,通常源於腫瘤微環境排斥免疫細胞等因素,使免疫系統難以辨識並啟動抗腫瘤反應。
因此,不同的免疫治療會採取不同策略:免疫檢查點抑制劑主要是解除對T細胞的「煞車」,讓原本已存在的免疫反應重新啟動;CAR-T療法則是將患者的T細胞加以改造,使其能更精準地辨識並攻擊癌細胞;而腫瘤微環境調控則著重於改變腫瘤周圍的環境,幫助免疫細胞進入腫瘤,甚至將原本的冷腫瘤轉變為較容易被免疫系統攻擊的狀態,進一步提升治療效果。
2. 腫瘤微環境調控劑 (Tumor Microenvironment Regulators, TMRs) 篩選平台
腫瘤免疫療法已成為晚期癌症最有前景的治療策略,其核心在於重新激活病患免疫系統,使原本的免疫逃避機制被逆轉,釋放能撲殺腫瘤的T細胞攻擊腫瘤並建立免疫記憶。
歷經十年的發展,腫瘤免疫療法主要以免疫檢查點抑制劑為主。新世代策略開始著重於重塑腫瘤微環境,如anti-PD-1/VEGF或anti-PD-L1/VEGF雙特異抗體,雖可增強抗血管新生效果,但對冷腫瘤的免疫活化仍有限。冷腫瘤患者的治療需求未被充分滿足,仍需聯合X藥物以加強腫瘤微環境重編程,以提升腫瘤免疫治療效益。
3. 新一代表觀免疫活化劑新藥篩選平台
表觀遺傳為在不改變去氧核糖核酸DNA序列的前提下,基因表現如何發生可遺傳的變化。因此在癌症治療上,表觀免疫活化劑為透過改變癌細胞的表觀遺傳標記,讓原本隱身的癌細胞顯形,並重新啟動被壓抑的免疫反應使T細胞發揮其作用以取代傳統化療之方式,同時達到對病人身體造成最小傷害及有效治療之目的。
表觀遺傳調控劑例如HDACi的開發至今至少有20年的時間,屬於一種標靶藥物,全球已有多個藥物獲得批准上市。但並不是每個表觀遺傳調控藥物都具有免疫調控活性(調節、改變或重塑免疫系統反應的能力)。華上生醫研發團隊發現,不同結構的表觀遺傳調控藥物具有不同的免疫調控活性。免疫調控在腫瘤免疫療法中和抗癌活性有關,因此,同時具有表觀遺傳與免疫調控活性將在腫瘤免疫療法的藥物開發上是重要的。
華上生醫研發團隊自主開發的新一代表觀免疫活化小分子藥物GNTbm-38,透過化學結構優化與電腦模擬運算,提升表觀遺傳調控及免疫調控活性,以加強腫瘤微環境的調控。
在多種免疫健全腫瘤動物模型中,經口服給藥後,GNTbm-38展現卓越的腫瘤免疫活化能力。與特定多重激酶抑制劑聯合使用,即可在極低劑量下全面喚醒免疫系統,達到極高的客觀緩解率(objective response rate, ORR)。
在Re-challenge實驗中,研究者將已被GNTbm-38治癒的小鼠再次植入腫瘤,結果顯示這些小鼠的免疫系統能立即識別並清除新腫瘤,證明GNTbm-38不僅能消滅現有腫瘤,還能建立長期免疫記憶,防止腫瘤復發。
GNTbm-38專利已完成全球多國申請,目前在41個國家獲得批准。臨床前研究已完成,並於2025年底向美國、台灣與中國提交IND申請,2026年正式啟動多國臨床一期試驗。GNTbm-38是華上生醫自主開發的口服腫瘤免疫療法核心藥物之一,代表公司在新一代腫瘤免疫治療領域的關鍵創新。
GNTbm-38抗腫瘤生長及重塑腫瘤微環境調控機制:
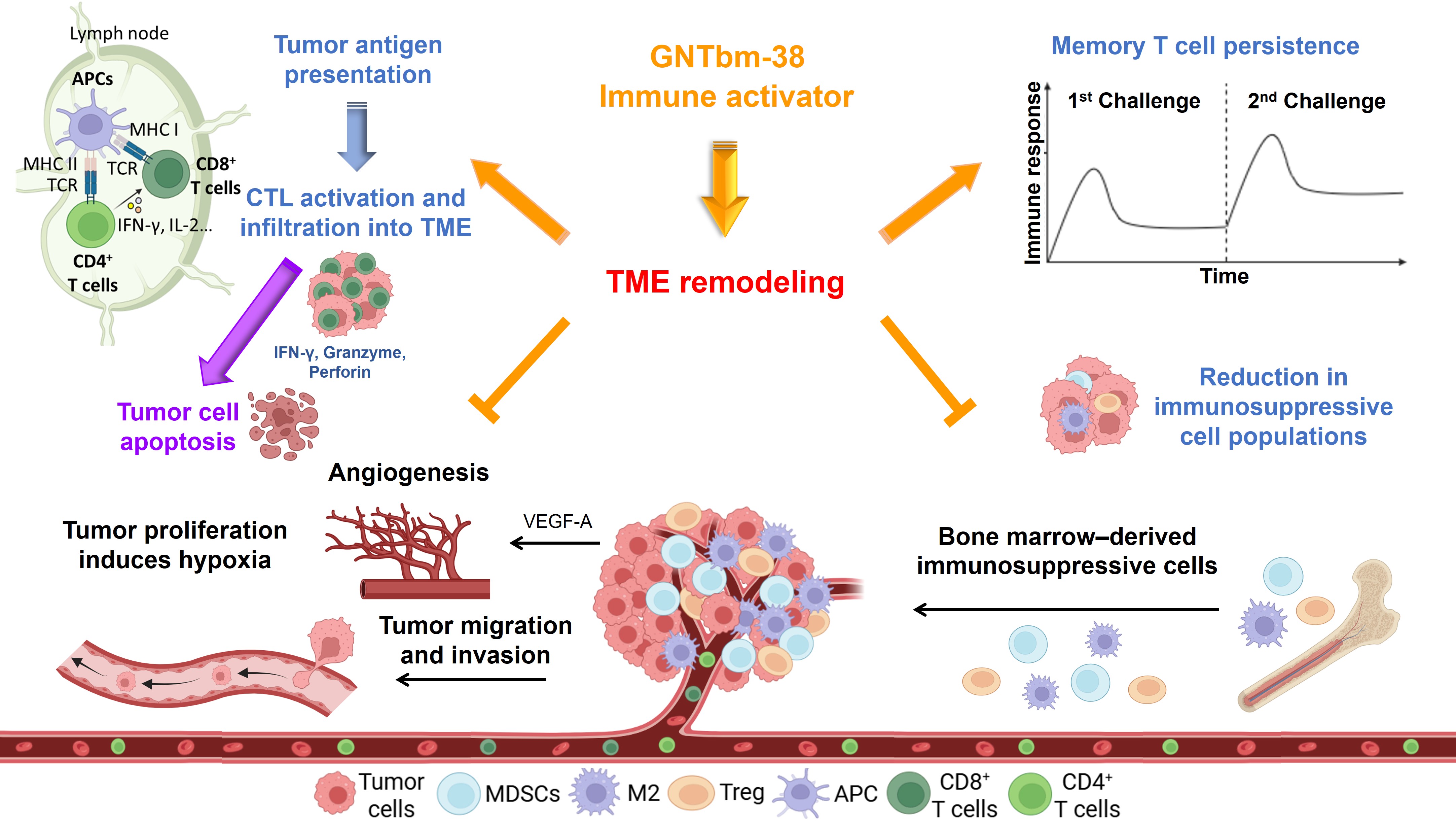
4. 免疫調控的多重激酶抑制劑篩選平台
多重激酶抑制劑(Tyrosine Kinase Inhibitor, TKI)為目前臨床上重要的抗癌標靶藥物之一,全球已有多項藥物成功上市。華上生醫研究發現,特定類型的TKI除抑制腫瘤生長外,亦具有強效免疫調控能力,可調節並重塑免疫系統反應,有助於改善腫瘤微環境。當此類TKI與GNTbm-38聯合使用時,可進一步喚醒宿主免疫系統,透過腫瘤微環境重編程,產生顯著的抗腫瘤免疫效果,並建立長期免疫記憶,達到持久緩解、不易復發的治療效益。
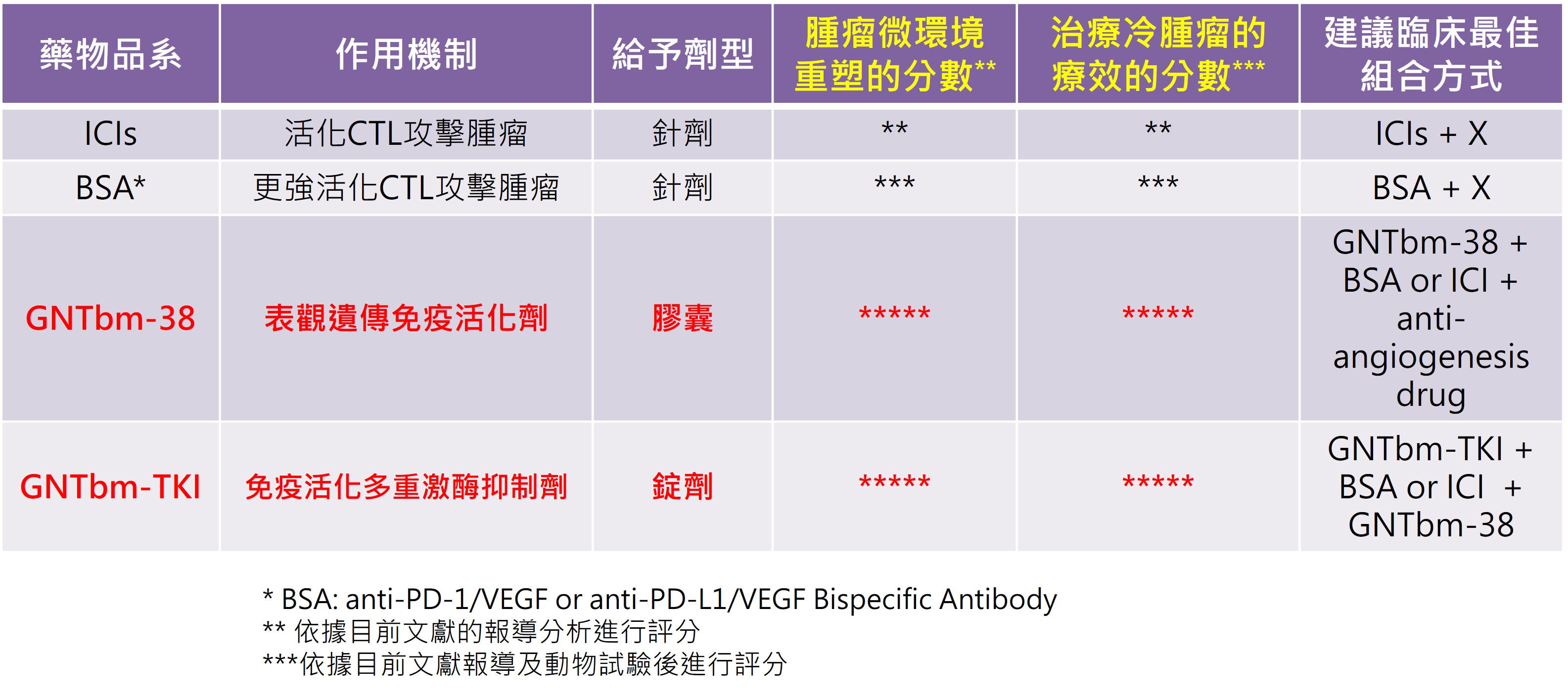
不同於傳統需依賴免疫檢查點抑制劑的治療策略,此創新組合可在不使用免疫檢查點抑制劑的情況下,透過多重機制全面重塑腫瘤微環境,包括促進腫瘤血管正常化、改善缺氧狀態、降低乳酸堆積,並有效促進具辨識與殺傷能力的細胞毒性T細胞(CTL)浸潤,同時抑制免疫抑制型細胞與調控細胞因子與趨化因子表現。華上生醫將以「GNTbm-38 + Y」作為核心治療策略,其中Y可為特定TKI,而以自主開發的GNTbm-TKI預期可達最佳治療效果。
基於多年研發基礎,華上生醫已成功開發具全新化學結構的多重激酶抑制劑GNTbm-TKI,靶向TYRO3、AXL、c-MER、BTK、ROS1、NTRK2、MET及VEGFR2等多個關鍵路徑,展現卓越的免疫調控潛力。動物試驗結果顯示,GNTbm-TKI與GNTbm-38聯合使用可達80%以上的客觀緩解率(ORR),並使免疫系統「記住」腫瘤,在後續再次植入腫瘤時時仍能快速清除腫瘤,達到長期抑制腫瘤生長且不復發的效果。目前研發團隊正持續推進更多動物試驗以驗證其療效。
此外,GNTbm-TKI已完成全球53個國家的專利申請,並進入臨床前開發階段,預計於2026年底完成美國、台灣與中國之IND申請,朝臨床試驗邁進。
GNTbm-TKI抑制癌細胞生長/侵犯與轉移/腫瘤血管新生及重塑腫瘤微環境調控機制: