表觀免疫活化劑
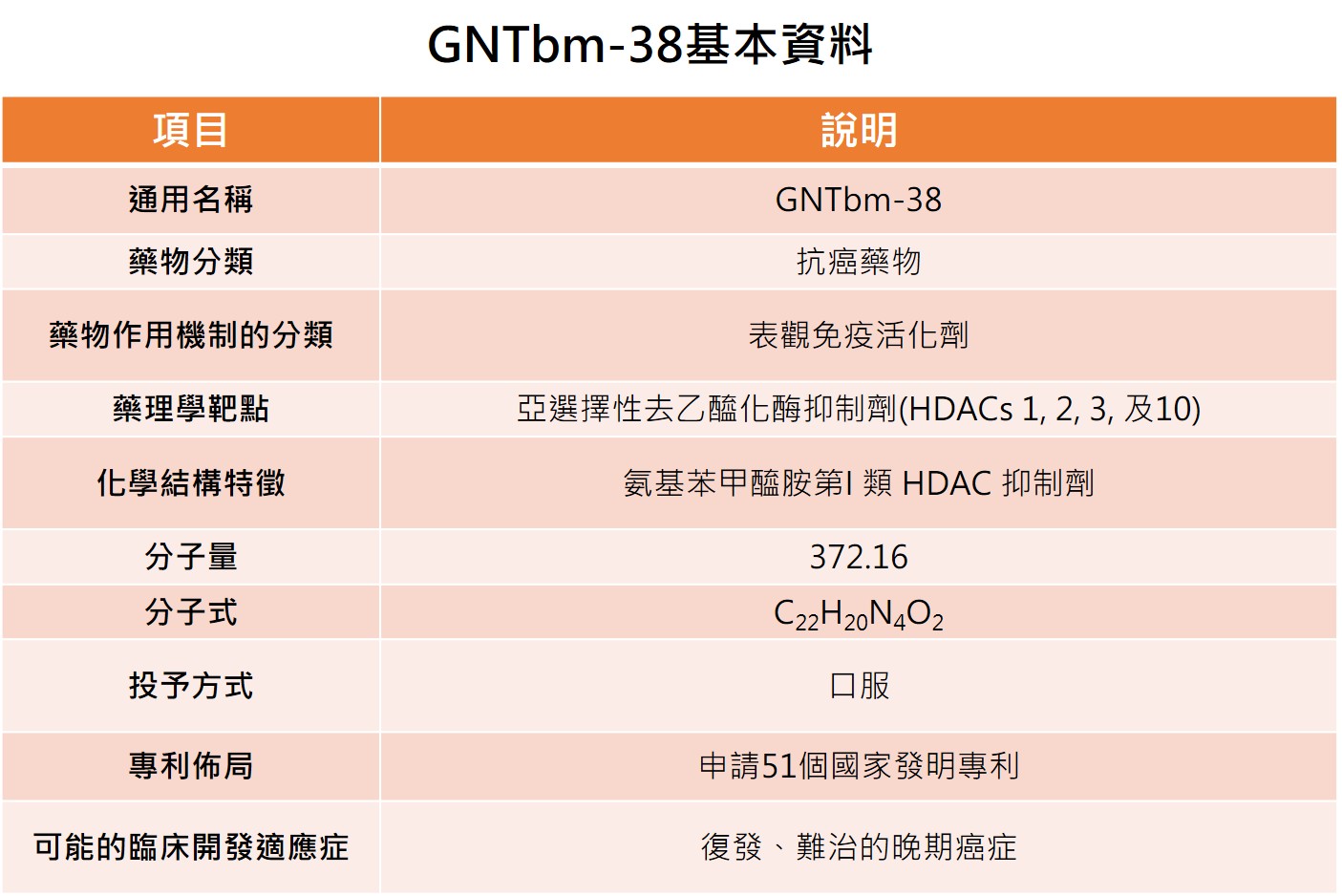
華上生醫研發團隊歷經多年研究,成功研發出全新結構之表觀免疫活化劑 GNTbm-38。該藥物為一種具創新性的小分子口服藥,兼具表觀遺傳調控與免疫調節的雙重功能。
GNTbm-38屬於苯醯胺類化合物,為選擇性 class I HDAC 抑制劑,目前已取得包含美國在內的多國發明專利。其作用機制使其具備成為腫瘤免疫治療「骨幹藥物(backbone therapy)」的潛力,可單獨使用或作為聯合治療核心。
在酵素、細胞及動物實驗中,GNTbm-38展現出優越的表觀遺傳調控與免疫活化能力。進一步研究顯示,當與特定靶點抑制劑(tyrosine kinase inhibitor, TKI)或免疫檢查點抑制劑(immune checkpoint inhibitor, ICI)聯合使用時,可有效重塑腫瘤微環境,顯著提升腫瘤治療反應率。
在臨床開發方面,GNTbm-38已完成臨床前試驗,並於2026年2月獲得美國FDA批准進入第一期臨床試驗以評估安全性,並進一步推進至第二期臨床試驗。首個適應症將鎖定復發/難治型外周T細胞淋巴瘤(R/R PTCL),並規劃申請美國孤兒藥資格。
未來在取得R/R PTCL藥證後,將進一步拓展至多種晚期實體腫瘤,採用「GNTbm-38 + Z」的聯合治療策略,其中Z可為特定靶點抑制型TKI或anti-PD-1/VEGF雙特異性抗體,以提升整體抗腫瘤療效。
1. GNTbm-38的第一個適應症---R/R PTCL(復發或難治型外周 T 細胞淋巴瘤)
過去多年的研究已證實,外周T細胞淋巴瘤(R/R PTCL)具有高度侵襲性與顯著的疾病異質性,且其發病機制與表觀遺傳調控失衡密切相關。因此,已有多種HDAC抑制劑進入臨床開發,並成功獲准用於R/R PTCL的治療,例如 Belinostat、Romidepsin 與 Tucidinostat。
相較於B細胞淋巴瘤,T細胞淋巴瘤的治療更具挑戰性,主要因為其缺乏標準治療方案、亞型多樣且異質性高,導致整體預後不佳,臨床上仍存在高度未被滿足的醫療需求。
在臨床前研究中,GNTbm-38於小鼠R/R AITL PDX模型中展現出顯著療效。與正對照組使用之 Belinostat 針劑相比,GNTbm-38以口服給藥即呈現更優異的抗腫瘤效果,進一步支持其作為單藥治療R/R PTCL的潛力。
在臨床開發策略上,華上生醫規劃
(1) 臨床Ia期試驗:收納晚期實體腫瘤患者,進行劑量爬升試驗,以評估劑量限制毒性(dose limiting toxicity, DLT)、最大耐受劑量(maximum tolerated dose, MTD)及二期推薦劑量(recommended phase 2 dose, RP2D)。
(2) 臨床Ib期試驗:於多國收納R/R PTCL患者,進一步評估療效與安全性。
若臨床結果符合預期,將以該試驗數據向美國、歐盟、日本及中國申請孤兒藥資格(orphan drug designation, ODD)。
在取得多國孤兒藥資格後,GNTbm-38將進一步申請快速審查(Fast Track)或類似加速機制,並規劃執行一項樞紐性II期臨床試驗(pivotal Phase II study),於美國、加拿大、澳洲、歐洲、日本、台灣及中國同步收案。
若該試驗顯示具備良好的療效與安全性,將據此向多國主管機關遞交新藥上市申請(new drug application, NDA),以提供R/R PTCL患者嶄新的治療選擇。
2. GNTbm-38的新增適應症---MYC/BCL2 DE-DLBCL(MYC 與 BCL2 高表達之瀰漫性大 B 細胞淋巴瘤)
瀰漫性大B細胞淋巴瘤(DLBCL)過去超過20年主要以標準治療方案 R-CHOP 作為第一線治療,其完全緩解率(CR)約為60–70%。然而,近年研究顯示DLBCL具有高度異質性,且與表觀遺傳調控失衡密切相關,進一步影響治療反應與預後。
其中,高級別B細胞淋巴瘤(high-grade B-cell lymphoma)若同時帶有MYC、BCL2及BCL6基因重排(double-hit或triple-hit lymphoma),預後極差,但此類病患比例僅約5–8%。相較之下,另一類**MYC/BCL2蛋白高表達的DLBCL(MYC/BCL2 DE-DLBCL)**約占30%,為臨床上更具規模的重要族群。儘管世界衛生組織(WHO)尚未將其列為獨立亞型,但此類患者接受 R-CHOP 治療時CR率較低,且5年無進展存活期(PFS)與總生存期(OS)均顯著劣於非高表達患者,顯示其高度未被滿足的醫療需求。
2024年,Tucidinostat 聯合 R-CHOP 已被證實可顯著提升MYC/BCL2 DE-DLBCL患者的第一線治療CR率(由61.8%提升至73%),且主要療效指標EFS達統計顯著差異,並已於中國取得新增適應症,驗證了表觀遺傳調控作為治療策略的臨床可行性。
在此基礎上,華上生醫進一步開發具差異化優勢的GNTbm-38,其為選擇性class I HDAC抑制劑,除具備更佳的抗腫瘤活性外,亦具有免疫調節能力,有望同時調控腫瘤細胞增生與腫瘤免疫微環境。
相較於 Tucidinostat,GNTbm-38具備更強的表觀遺傳重新編程能力與潛在更佳的治療反應深度,目標將CR率進一步提升至85%。
根據世界衛生組織(WHO)定義,MYC蛋白表現量高於40%、BCL2高於50%即屬高表達族群。
由於MYC高表達促進腫瘤細胞增生,而BCL2高表達抑制細胞凋亡,兩者共同作用使腫瘤對 R-CHOP 產生抗性,因此達到完全緩解(CR)對於延長PFS與OS至關重要。
基於上述機制與臨床需求,華上生醫提出創新的分層治療策略,以GNTbm-38作為治療骨幹(backbone therapy),結合 BTK inhibitor 與 Rituximab:
(1) 若患者在前兩個治療週期接受 GNTbm-38 + BTK抑制劑 + Rituximab 即達到CR,則持續該組合治療6個週期,以降低化療暴露。
(2) 若僅達部分緩解(PR)或疾病穩定(SD),則進一步加入 CHOP 進行6個週期治療,以提升至CR。
此策略可依據早期治療反應進行調整,兼顧療效最大化與毒性管理,並充分發揮GNTbm-38在提升CR率、降低抗藥性及作為聯合治療平台的潛力,為MYC/BCL2 DE-DLBCL患者提供更具突破性的治療選擇。
3. GNTbm-38的新增適應症---MSS/pMMR mCRC(微衛星穩定型之轉移性大腸直腸癌)
大腸直腸癌(CRC)為全球主要致死癌症之一,每年新診斷病例約200萬人,死亡人數約110萬人,臨床未滿足需求極高。現行腫瘤免疫療法主要僅對微衛星不穩定高(MSI-H)族群有效,然而此類患者僅約佔5%,絕大多數患者(約90%)屬於微衛星穩定型(MSS/pMMR),對免疫治療反應不佳,形成典型的「免疫冷腫瘤」困境。
對於無法手術切除的晚期大腸直腸癌(mCRC),目前主要依賴全身性治療,但MSS/pMMR患者缺乏有效的免疫治療選項。此一治療瓶頸於2024年出現突破:Tucidinostat 聯合 anti-PD-1 antibody 及 Bevacizumab 的三聯療法,可透過表觀遺傳調控與血管生成抑制的協同作用,有效重塑腫瘤微環境,將MSS型mCRC由免疫冷腫瘤轉化為免疫熱腫瘤,使客觀反應率(ORR)提升至44%,中位無進展存活期(mPFS)達7.3個月,創下歷史性成果。
目前該三聯療法已進入樞紐性III期臨床試驗,以 Fruquintinib 為對照組,並以總生存期(mOS)為主要終點,預期有機會取得正向結果,進一步驗證此一「表觀遺傳 × 免疫 × 抗血管生成」策略的臨床價值。
在此基礎上,GNTbm-38作為新一代表觀遺傳調控劑,相較於 Tucidinostat 展現出更強的腫瘤免疫活化能力與表觀遺傳重新編程效果,有望進一步提升免疫治療反應率。GNTbm-38將採用創新聯合策略,結合anti-PD-1/VEGF雙特異性抗體,同時達成免疫檢查點阻斷與腫瘤血管調控,預期可在提升療效的同時降低多藥併用所帶來的副作用。
臨床開發上,GNTbm-38將鎖定晚期大腸直腸癌第三線治療,針對MSS/pMMR患者進行概念驗證(proof-of-concept, POC)。透過其獨特的免疫活化機制,GNTbm-38可作為聯合治療的骨幹藥物(backbone therapy),與雙特異性抗體產生協同作用,進一步強化腫瘤微環境重塑能力。
此策略不僅有望突破MSS型大腸直腸癌長期以來對免疫治療不敏感的限制,也將成為GNTbm-38在晚期實體腫瘤「冷腫瘤轉熱腫瘤」應用中的關鍵臨床驗證,展現其作為平台型免疫調節藥物的核心價值。