強效免疫調控多重激酶抑制劑
過去20年間,已有多種多重激酶抑制劑(tyrosine kinase inhibitors, TKIs)獲准上市,用於治療多種癌症及其他適應症。然而,現有TKI多以直接抑制腫瘤生長或血管新生為主要機制,對於腫瘤免疫微環境(tumor microenvironment, TME)的調控能力相對有限。
有鑑於此,華上生醫研發團隊聚焦於開發具備強效免疫調節能力的新一代多重激酶抑制劑,並成功自主開發出具有全新結構的免疫調控型TKI —— GNTbm-TKI,旨在應用於腫瘤免疫治療。
GNTbm-TKI為經多年研究篩選出的創新小分子口服候選藥物,具備優異的免疫調節活性。在酵素、細胞與動物實驗中,GNTbm-TKI展現出多重免疫相關訊號通路的調控能力,可同時抑制多個與腫瘤免疫逃脫及免疫抑制相關的關鍵激酶,包括TYRO-3、AXL、c-MER(TAM family)、BTK、ROS1、NTRK2、VEGFR2及MET。此一多靶點設計使其不僅可抑制腫瘤生長與血管新生,亦可有效重塑免疫抑制性腫瘤微環境。
進一步研究顯示,GNTbm-TKI與HDAC抑制劑(如GNTbm-38)聯合使用時,具有顯著的協同作用,可透過「表觀遺傳調控 × 激酶訊號調控」雙重機制,將免疫冷腫瘤轉化為免疫熱腫瘤,大幅提升腫瘤免疫應答率。此一特性使GNTbm-TKI不僅具備單藥活性(如應用於晚期神經內分泌瘤),更具備作為聯合治療骨幹藥物(combination backbone therapy)的潛力。
相較於傳統TKI,GNTbm-TKI的競爭優勢在於其免疫導向的多靶點設計,可同時影響腫瘤細胞、腫瘤血管及免疫細胞(如巨噬細胞與樹突細胞),進一步提升免疫檢查點抑制劑的治療效果。因此,GNTbm-TKI可靈活應用於多種聯合策略,包括:
(1) 與HDAC抑制劑(如 Tucidinostat 或GNTbm-38)聯合
(2) 與免疫檢查點抑制劑(anti-PD-1/PD-L1)聯合
(3) 與anti-PD-1/VEGF bispecific antibody 聯合
透過上述策略,GNTbm-TKI有望成為腫瘤免疫治療的關鍵藥物,廣泛應用於多種晚期實體腫瘤。
在臨床開發方面,GNTbm-TKI目前已進入臨床前研究階段,預計於2027年進入臨床一期試驗。後續將優先與GNTbm-38進行聯合開發,推進至臨床二期試驗,並以孤兒藥適應症作為切入點,透過單臂樞紐性II期試驗加速取得藥證。
整體開發策略將以「GNTbm-TKI + I(Immunotherapy)」為核心,其中I涵蓋HDAC抑制劑、免疫檢查點抑制劑及雙特異性抗體等多元免疫治療工具。藉由其強效的腫瘤免疫調控能力,GNTbm-TKI有望突破多種實體腫瘤中免疫冷腫瘤的治療限制,並建立具擴展性的腫瘤免疫治療平台。
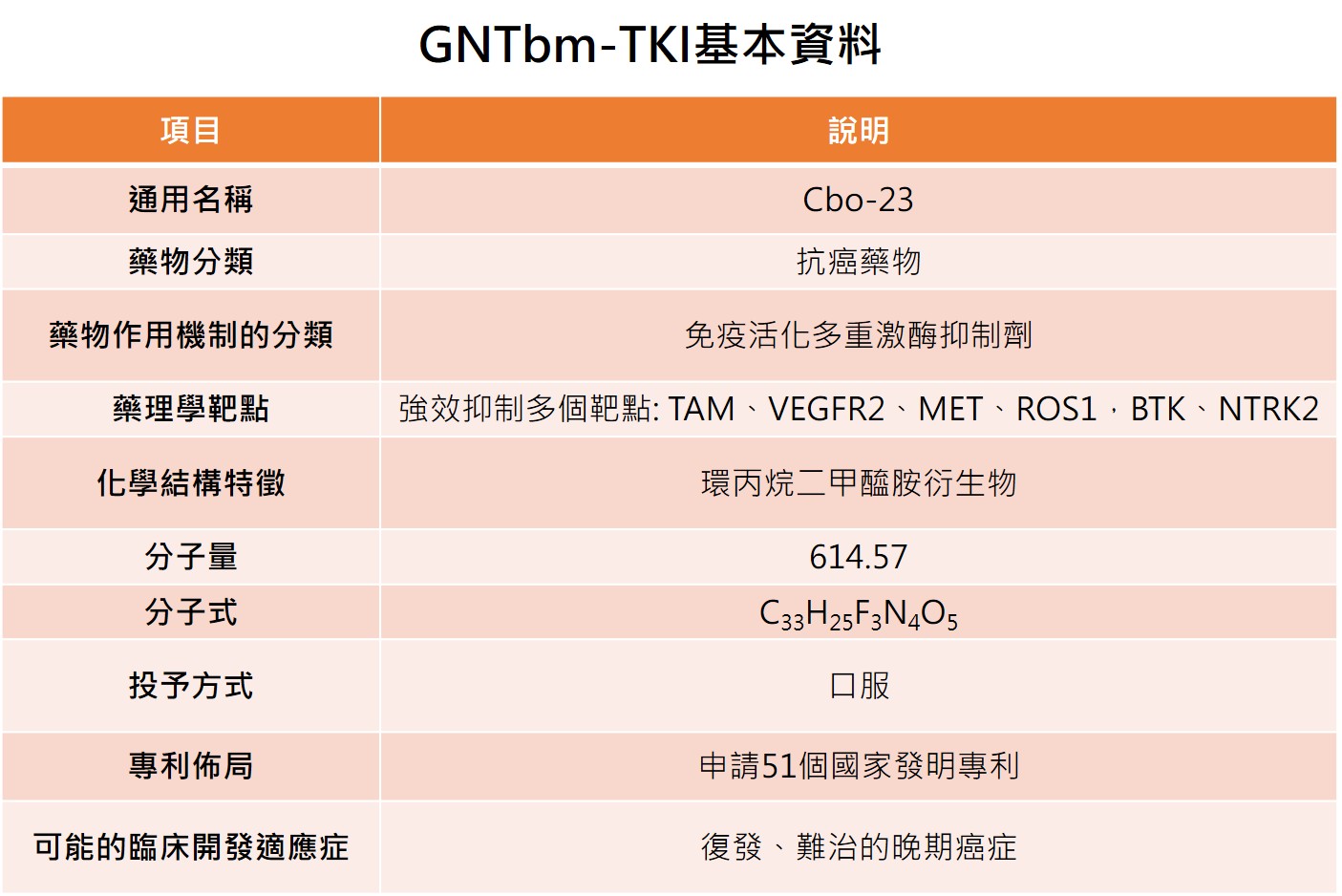
1. GNTbm-TKI的第一個適應症---神經內分泌瘤
神經內分泌腫瘤(neuroendocrine tumor, NET)為一類相對罕見但具臨床挑戰性的腫瘤,起源於具神經與內分泌雙重功能的細胞,多數具有惡性潛力。NET最常發生於胃腸道,其次為肺部(約30%發生於支氣管系統),另約7%發生於胰臟,稱為胰臟神經內分泌腫瘤(pNET)。
根據市場研究資料(Datamonitor Healthcare)顯示,2024年全球NET病例約為588,200例,預計至2031年將成長至679,400例,其中亞洲佔最大比例(約357,600例)。此外,NET發生率於北美、亞洲與歐洲均呈持續上升趨勢,以United States為例,過去40年間發生率已增加超過6倍,顯示此疾病的臨床與市場需求正快速擴大。
在治療方面,2025年4月,Cabozantinib 獲 U.S. Food and Drug Administration 批准,用於治療局部晚期或轉移性且無法手術切除之分化良好pNET與胰外NET(epNET)。此類多重激酶抑制劑(如 Cabozantinib 與 Zanzalintinib)主要透過抑制TAM family、VEGFR2及c-MET等訊號通路,達到抑制腫瘤生長、血管新生、侵襲轉移及部分免疫調節的效果,已成為NET重要的系統性治療選項。
在此基礎上,GNTbm-TKI作為新一代免疫調控型多重激酶抑制劑,展現出明顯的差異化優勢。除了涵蓋TAM、VEGFR2與c-MET等關鍵靶點外,GNTbm-TKI對ROS1、BTK、NTRK2及Tie2等免疫與腫瘤相關訊號具有更強的抑制活性,使其在抑制腫瘤生長與血管新生的同時,亦能更有效地重塑腫瘤免疫微環境。
相較於現有TKI(如 Cabozantinib 與 Zanzalintinib),GNTbm-TKI的核心競爭優勢在於其免疫導向的多靶點設計,可更全面調控腫瘤相關免疫抑制機制(如腫瘤相關巨噬細胞與B細胞訊號),進一步提升抗腫瘤免疫反應。
因此,GNTbm-TKI不僅具備作為NET單藥治療的潛力,更有望透過其強效免疫活化能力,進一步與表觀遺傳調控劑(如GNTbm-38)或免疫療法進行聯合應用,建立差異化的腫瘤免疫治療策略,並拓展至多種晚期實體腫瘤。
2. GNTbm-TKI的新增適應症開發採取一籃子開發策略---晚期腎癌、晚期頭頸癌、晚期大腸直腸癌
籃子式試驗(Basket Trial)是一種突破傳統癌器官分類的精準醫療臨床設計,其核心邏輯是「異病同治」:將患有不同癌症但皆具有相同基因突變或生物標記的患者納入同一個「籃子」中,給予同一種靶向藥物治療。這種設計能有效驗證藥物的廣譜性,加速達成概念驗證(POC),是開發針對特定表觀遺傳特徵之難治性癌症的高效路徑。
GNTbm-TKI、GNTbm-38與anti-PD-1/VEGF雙特異性抗體的三聯組合,代表一項具高度潛力的新一代腫瘤免疫治療策略。此組合透過「激酶訊號調控 × 表觀遺傳重新編程 × 免疫檢查點阻斷與血管調控」三重機制,協同作用於腫瘤細胞與腫瘤微環境(TME),達到全面性的抗腫瘤效果。
在臨床前研究中,GNTbm-TKI與GNTbm-38聯合已被證實可顯著重塑腫瘤微環境並活化免疫反應,展現優異的抗腫瘤活性。此外,GNTbm-38與anti-PD-1 antibody聯合亦已驗證具有顯著的腫瘤抑制效果。基於上述結果,進一步整合為三聯療法(GNTbm-TKI + GNTbm-38 + anti-PD-1)後,展現出更為強化的腫瘤免疫活化與抗癌效果,支持其高度協同潛力。
在免疫治療策略上,相較於傳統anti-PD-1 antibody聯合Bevacizumab的雙藥組合,anti-PD-1/VEGF雙特異性抗體可同時阻斷免疫檢查點與腫瘤血管生成訊號,具備更佳的藥效整合性與潛在較低的治療負擔。因此,將其納入三聯組合,有望進一步提升療效並優化安全性。
綜合機制與臨床前證據,GNTbm-TKI + GNTbm-38 + anti-PD-1/VEGF雙特異性抗體的三聯療法具備強效腫瘤免疫活化與腫瘤微環境重塑能力,可望應用於多種晚期實體腫瘤,初步優先適應症包括:
(1) 晚期腎細胞癌(第一線治療)
(2) 晚期頭頸癌(第一線治療)
(3) 晚期大腸直腸癌(第二線治療)
在臨床開發策略上,針對此三聯組合,將採用籃子式試驗(basket trial)設計,同時評估多種腫瘤適應症的療效與安全性。初期規劃於各適應症收納約20位患者,以進行概念驗證(proof-of-concept, POC)。
若試驗達成預設之主要療效指標,將進一步推進至樞紐性第三期臨床試驗(pivotal Phase III study),並採取多國多中心收案策略,涵蓋美國、歐盟、加拿大、澳洲、台灣、中國及日本,以全面驗證其療效與安全性,並加速全球臨床開發與上市進程。