氟吡苯醯胺 (Tucidinostat/Chidamide)
Tucidinostat在台灣的第一個適應症 - 合併Exemestane用於治療HR陽性, Her-2陰性晚期乳癌
1. 剋必達®在台灣開發10年獲得國產新成分新藥的藥證
氟吡苯醯胺的台灣商品名為剋必達®(英文成名:Tucidinostat),為新一代口服表觀遺傳調控劑(Epigenetic Modulator),是一種亞選擇性HDAC抑制劑,華上生醫耗時10年,投入數億研發成本,取得國產新成分新藥的藥證。
.jpg)
2. Tucidinostat滿足HR+/Her-2-晚期乳癌第二線治療
依據NCCN治療指南及台灣乳房醫學會專家共識,HR+/Her-2-晚期乳癌第一線治療主要推薦以內分泌療法聯合CDK4/6抑制劑作為標準治療。另又依據台灣健保給付規定,HR+/Her-2-晚期乳癌病患終生可以健保給付使用CDK4/6抑制劑24個月,且依據國際文獻報導HR+/Her-2-晚期乳癌第一線治療使用內分泌療法聯合CDK4/6抑制劑都有非常優異的治療效益,mPFS約在24個月。這些理由都傾向於支持,約有70%台灣HR+/Her-2-晚期乳癌病患在第一線治療就會使用內分泌療法聯合CDK4/6抑制劑。
當第一線治療使用內分泌療法聯合CDK4/6抑制劑失敗後,會導致病患同時具有內分泌治療及CDK4/6抑制劑的雙重抗藥性發生,使得後續的第二線治療選擇將更有限。依據NCCN治療指南推薦,第二線治療能夠使用的藥物相當有限。
第一種推薦: 若病患從未使用過CDK4/6抑制劑,則第二線治療可以推薦使用CDK4/6抑制劑聯合內分泌療法;
第二種推薦: 若病患有PIK3CA突變發生,可以推薦使用Alpelisib (PI3Ki)合併fulvestrant;
第三種推薦: 病患可以使用Everolimus (mTORi)合併Exemestane。
Tucidinostat(HDACi)聯合 Exemestane 提供了晚期乳癌治療的另一種策略選擇。作為一種表觀遺傳調控藥物,Tucidinostat 可從基因表達層面進行較深層的調控,其作用機制與目前已核准的內分泌治療或 CDK4/6 抑制劑有所不同。從機轉上而言,Tucidinostat有潛力克服長期內分泌治療及 CDK4/6 抑制劑所導致的抗藥性問題。
基於此,華上生醫規劃於台灣執行一項真實世界研究(real-world study),針對 HR+/HER2- 晚期乳癌患者,在第一線接受內分泌治療合併 CDK4/6 抑制劑失敗後,於第二線治療使用 Tucidinostat 聯合 Exemestane,進一步評估其臨床治療效益。
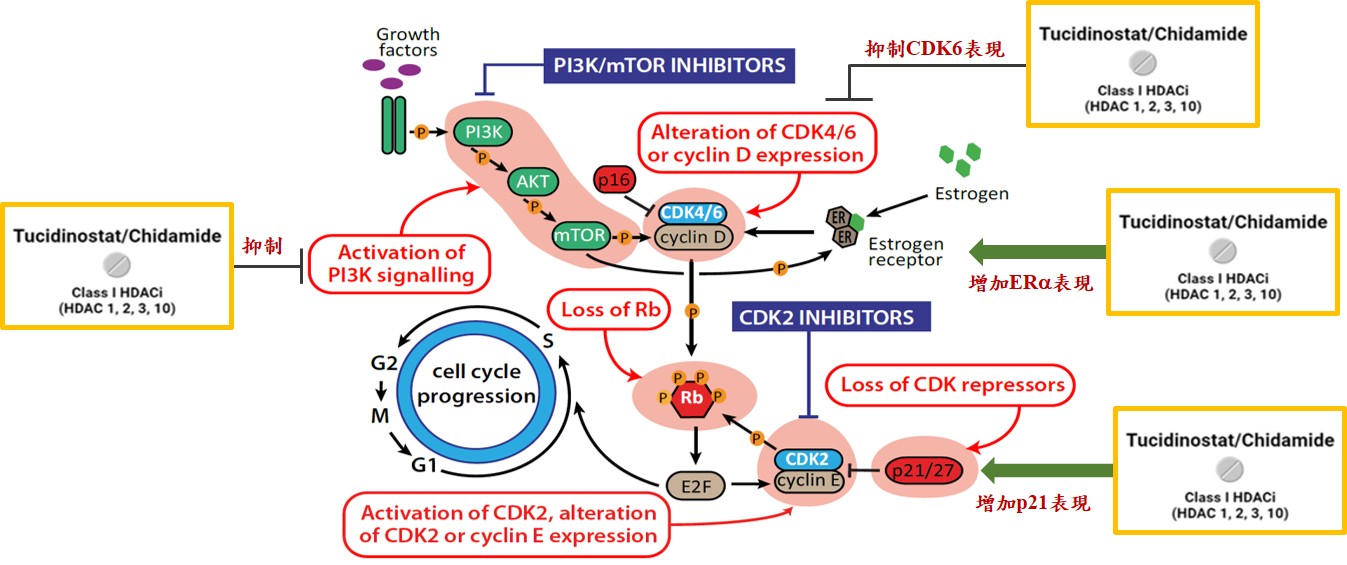
Tucidinostat可能改善第一線治療HR+/Her-2-晚期乳癌使用內分泌療法聯合CDK4/6抑制劑所產生的雙重抗藥性問題
Tucidinostat是唯一屬於多靶點基因調控的表觀遺傳調控劑,已被台灣乳房醫學會專家推薦為第二線治療的首選。
.jpg)
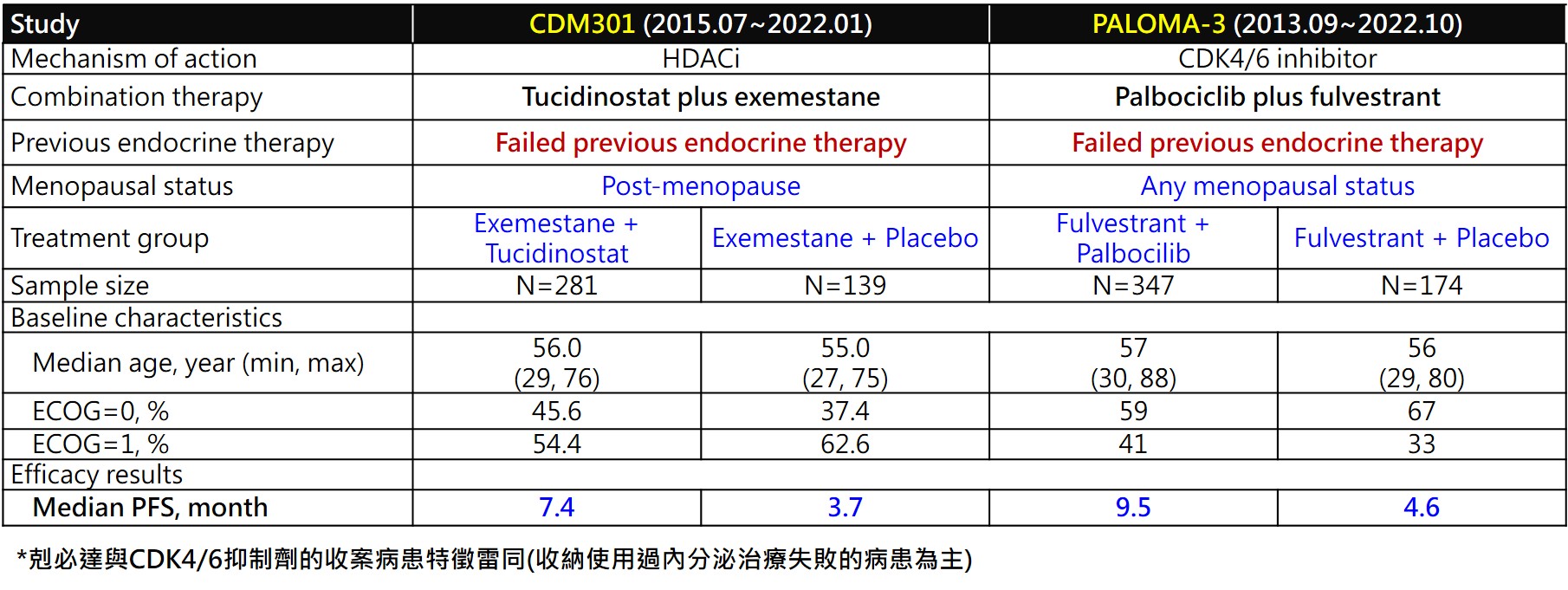
3. Tucidinostat用於治療HR+/HER-2-晚期乳癌樞紐臨床三期試驗(CDM301)
華上生醫遞交乳癌臨床三期試驗的計畫書給TFDA/CDE審查,並獲得TFDA/CDE建議,試驗的設計與收納病患條件與中國所執行的臨床試驗一樣,並建議台灣的臨床數據與中國的臨床數據合併作為本試驗的臨床試驗終點。
本試驗的臨床試驗名稱為CDM301,收納HR+/Her-2-晚期乳癌病患,既往使用過至少一次的內分泌療法治療失敗或復發的病患,使用Tucidinostat聯合Exemestane治療。依據入組病患的內臟轉移與否進行分層,並以2:1進行兩組的隨機分配,進入試驗組及安慰劑組,直到病患服用試驗藥物疾病進展或因藥物毒性無法耐受而退出試驗,主要療效指標以臨床研究者為主的PFS。試驗時間約5年。
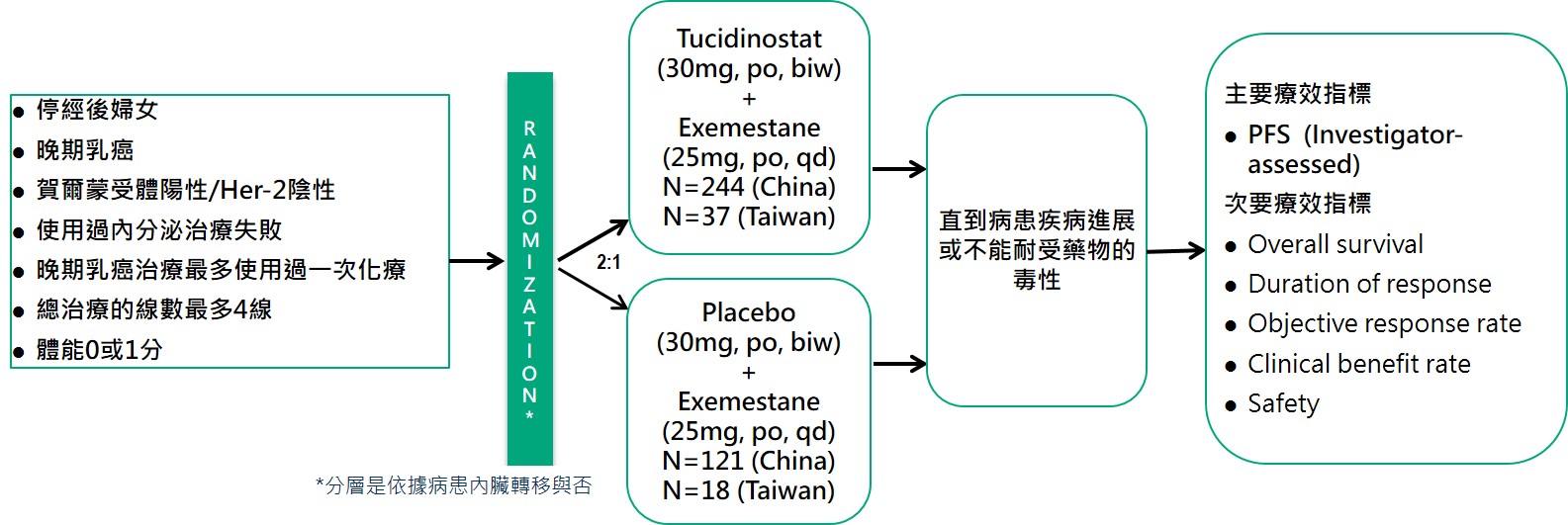
CDM301 為一項設計嚴謹的樞紐性第三期臨床試驗,採隨機、安慰劑對照、多中心設計,並於台灣與中國同步收案。全試驗共納入420名患者,依2:1比例隨機分配至 Tucidinostat 聯合 Exemestane(試驗組,n=281)或安慰劑聯合 Exemestane(對照組,n=139)。
在主要終點無惡化存活期(progression-free survival, PFS)方面,試驗組顯著優於對照組,其中位PFS分別為7.4個月與3.7個月(HR=0.716;95% CI, 0.562–0.911;P=0.0066),顯示 Tucidinostat 聯合治療可有效延緩疾病進展。
台灣子族群分析共納入55名患者,同樣以2:1隨機分配至試驗組(n=37)與對照組(n=18)。結果顯示,試驗組的中位PFS為8.6個月,對照組為3.7個月(HR=0.516;95% CI, 0.268–0.993;P=0.0477),呈現與整體族群一致且更為顯著的治療效益。
在次要終點方面,整體族群的客觀緩解率(objective response rate, ORR)於試驗組為16.73%,高於對照組的7.91%,且達統計顯著差異,進一步支持 Tucidinostat 聯合治療的臨床效益。